【28期】前沿靶点速递:每周医学研究精选
日期:2025-02-19 13:40:14
01.靶点:IL-27
应用:结直肠癌、肺癌等癌症潜在治疗靶点
来源:IL-27 elicits a cytotoxic CD8 + T cell program to enforce tumour control.Nature,2025 Feb 05
IL-27是一种关键的免疫调节因子,在肿瘤免疫治疗中展现出巨大潜力。研究表明,IL-27通过直接作用于肿瘤特异性CD8+ T细胞,增强其在肿瘤微环境中的持久性和效应功能,从而提升抗肿瘤免疫反应。在小鼠模型中,过表达IL-27或使用半衰期延长的IL-27蛋白可有效诱导肿瘤消退,且未观察到明显的免疫相关毒性。此外,IL-27与PD-L1抑制剂联合使用可显著增强治疗效果,为克服肿瘤免疫逃逸和耐受提供了新策略。临床数据进一步表明,IL-27的高表达与抗PD-1/PD-L1治疗的积极反应相关。这些发现揭示了IL-27在抗肿瘤免疫中的核心作用,并为其作为单一疗法或联合免疫治疗的临床应用奠定了重要基础。
02.靶点: CALCRL
应用:治疗2型糖尿病和肥胖相关代谢疾病的潜在靶点
来源:Endothelial insulin resistance induced by adrenomedullin mediates obesity-associated diabetes.Science,2025 Feb 07
《Science》杂志的一项新研究揭示了糖尿病的“隐形推手”——肾上腺髓质素(adrenomedullin)。该激素通过抑制血管内皮细胞的胰岛素信号传导,导致肥胖相关2型糖尿病患者的全身性胰岛素抵抗。研究发现,肾上腺髓质素激活Gαs-PKA-PTP1B信号通路,抑制胰岛素受体磷酸化,从而引发内皮胰岛素抵抗。在肥胖状态下,脂肪细胞大量分泌肾上腺髓质素,加剧了这一过程。通过阻断肾上腺髓质素受体,可以改善肥胖引起的胰岛素抵抗,为肥胖相关代谢疾病提供了新的治疗靶点。此外,内皮细胞可能成为多种疾病中胰岛素抵抗的共同节点,靶向内皮胰岛素信号通路具有广泛的治疗潜力。
03.靶点:HOXC4
应用:肥胖相关代谢疾病(如2型糖尿病)和胰腺癌的潜在治疗靶点
来源:Homeobox C4 transcription factor promotes adipose tissue thermogenesis.Diabetes,2025 Jan 24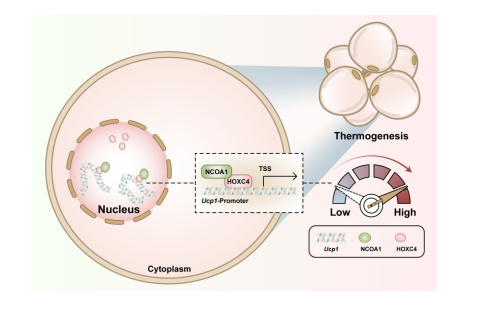
04.靶点:GITRL
应用:可用于开发针对实体肿瘤的新型CAR-T细胞疗法
来源:GITRL enhances cytotoxicity and persistence of CAR-T cells in cancer therapy.Mol Ther,2025 Jan 25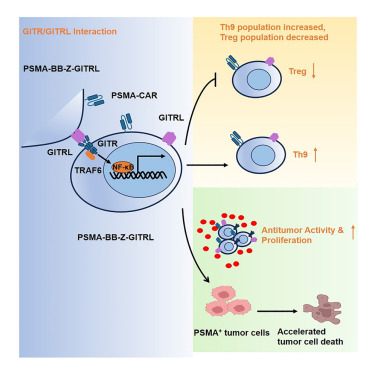
华东师范大学杜冰教授团队在《Molecular Therapy》发表研究,发现过表达GITRL的CAR-T细胞能显著增强实体肿瘤治疗效果。CAR-T疗法在血液恶性肿瘤治疗中取得突破,但在实体瘤治疗中效果不佳。GITR/GITRL信号能增强T细胞存活、增殖及杀伤功能。研究显示,过表达GITRL的CAR-T细胞可促进T细胞向抗肿瘤表型分化,增强激活及杀伤能力,促进增殖和Th9细胞分化,降低Treg细胞比例和耗竭。在前列腺癌动物模型中,过表达GITRL的CAR-T细胞延长了小鼠生存期,提升了持久性,且安全性较高。
05.靶点:LDHB
应用:治疗KRAS突变非小细胞肺癌(NSCLC)的潜在靶点
来源:Lactate dehydrogenase B noncanonically promotes ferroptosis defense in KRAS-driven lung cancer.Cell Death Differ,2024 Dec 07
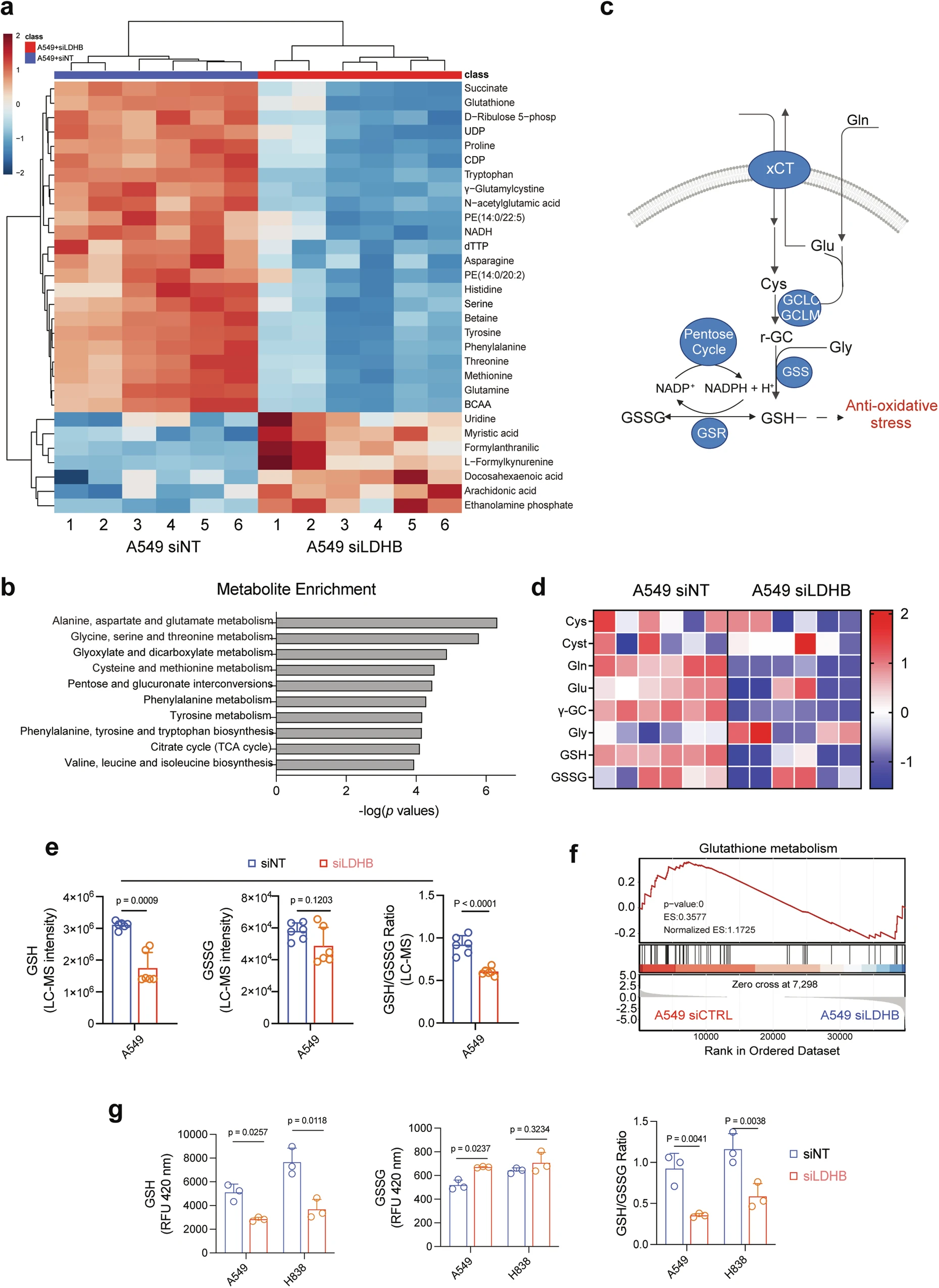
瑞士伯尔尼大学附属小岛医院研究团队在《Cell Death & Differentiation》杂志发表的研究发现乳酸脱氢酶B(LDHB)在KRAS驱动的非小细胞肺癌中通过非经典途径促进对铁死亡的抵抗。研究通过多组学整合分析,证实LDHB不仅参与乳酸-丙酮酸循环,还能调控谷胱甘肽合成及线粒体氧化磷酸化,维持氧化还原稳态。抑制LDHB并联合阻断SLC7A11可加剧线粒体代谢紊乱,引发脂质过氧化升高,诱发铁死亡。体外实验与小鼠模型显示,该策略能显著抑制肿瘤增殖并延长生存期,为KRAS突变肺癌的代谢治疗提供新思路。
06.靶点:MFGE8
应用:治疗多种肿瘤相关耐药问题的潜在靶点
来源:MFGE8 induces anti-PD-1-therapy resistance by promoting extracellular vesicle sorting of PD-L1.Cell Rep Med,2025 Jan 16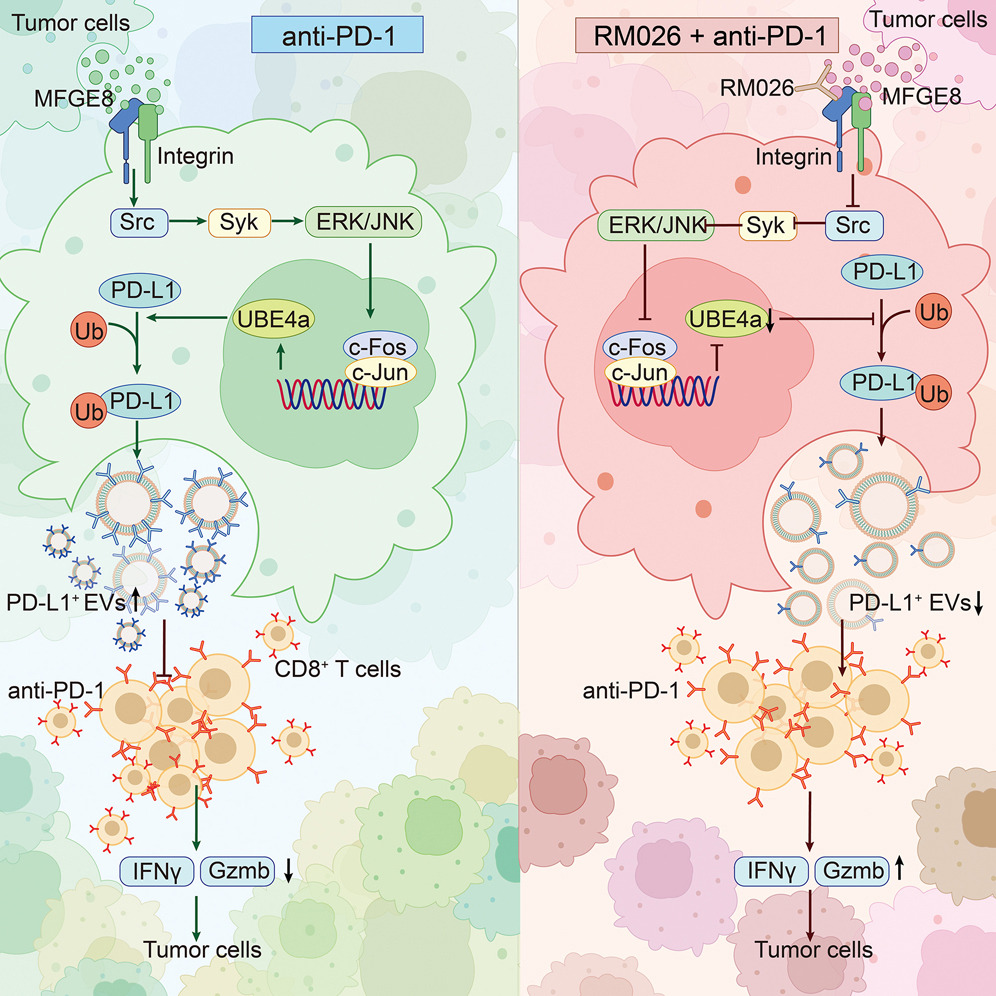
浙江大学蔡志坚教授团队在《Cell Reports Medicine》杂志发表研究,揭示了MFGE8(乳脂球表皮生长因子8)在介导抗PD-1治疗耐药中的关键作用。研究发现,肿瘤细胞通过分泌MFGE8诱导PD-L1分选至胞外囊泡(TEVs),进而增强免疫抑制能力,导致抗PD-1治疗耐药。团队还发现,MFGE8通过激活αv整合素信号通路,上调UBE4A的表达,促进PD-L1的泛素化和分选至TEVs。在肿瘤进展过程中,MFGE8水平升高,进一步加剧了抗PD-1治疗的耐药性。
从临床转化角度来看,使用抗MFGE8中和抗体可以有效下调UBE4A和TEVs上的PD-L1,从而消除抗PD-1治疗耐药性。此外,肿瘤患者血清中MFGE8和PD-L1+ EV水平呈正相关,其高水平与抗PD-1治疗后的不良预后相关。因此,MFGE8不仅是一个有潜力的抗耐药靶点,还可作为预测抗PD-1治疗反应性的生物标志物。
07.靶点:HCAR1
应用:治疗结肠直肠癌及其他多种癌症的潜在靶点
来源:The lactate receptor HCAR1 drives the recruitment of immunosuppressive PMN-MDSCs in colorectal cancer.Nat Immunol,2025 Feb 04
华东师范大学生命科学学院卢伟强研究员和刘明耀教授团队在《Nature Immunology》杂志发表研究,揭示了G蛋白偶联受体家族成员HCAR1通过感知乳酸信号,驱动肿瘤免疫逃逸的新机制。研究发现,乳酸受体HCAR1信号通路的激活会诱导结肠直肠肿瘤细胞中趋化因子CCL2和CCL7的表达,从而招募免疫抑制性CCR2+多形核髓系来源的抑制细胞(PMN-MDSCs)进入肿瘤微环境。在结肠直肠癌小鼠模型中,敲除Hcar1基因显著降低了肿瘤浸润性CCR2+ PMN-MDSCs的数量,增强了CD8+ T细胞的活化,从而减轻了肿瘤负担。此外,FDA批准的药物利血平可抑制乳酸介导的HCAR1激活,削弱PMN-MDSCs的募集,增强CD8+ T细胞依赖的抗肿瘤免疫反应,并使免疫疗法耐药的肿瘤对PD-1抗体疗法敏感。该研究为理解乳酸介导的肿瘤免疫逃逸机制提供了新视角,并为开发肿瘤免疫创新疗法提供了新靶点和候选药物。
08.靶点:FBP1
应用:治疗肝细胞癌(HCC)的潜在靶点
来源:FBP1 controls liver cancer evolution from senescent MASH hepatocytes.Nature,2025 Jan

加州大学圣地亚哥分校的Michael Karin、Li Gu和Yahui Zhu团队在《Nature》杂志发表研究,揭示了FBP1(果糖-1,6-二磷酸酶1)在肝细胞癌(HCC)发生中的关键作用。研究发现,FBP1是一个p53靶基因,在代谢功能障碍相关脂肪性肝炎(MASH)诱导的衰老肝细胞中表达上调,但在大多数人类HCC中通过启动子高甲基化和蛋白酶体降解被抑制。
FBP1在代谢应激的癌前病变肝细胞和HCC祖细胞中率先下降,与AKT和NRF2的致癌激活同时发生。AKT和NRF2通过加速FBP1和p53的降解,增强了衰老HCC祖细胞的增殖和代谢活性。这种NRF2-FBP1-AKT-p53代谢开关不仅逆转了衰老,还促进了MASH向HCC的进展,并增强了DNA损伤诱导的体细胞突变积累。
该研究指出,FBP1的缺失是MASH向HCC进展的关键机制,为HCC的预防和治疗提供了新的靶点。
09.靶点:CERT
应用:治疗急性髓系白血病(AML)的潜在靶点
来源:Targeting CERT sensitizes AML Cells to FLT3 Inhibitors through activating GRP78-ATF6-CHOP Axis .Nat Commun,2025 Feb 04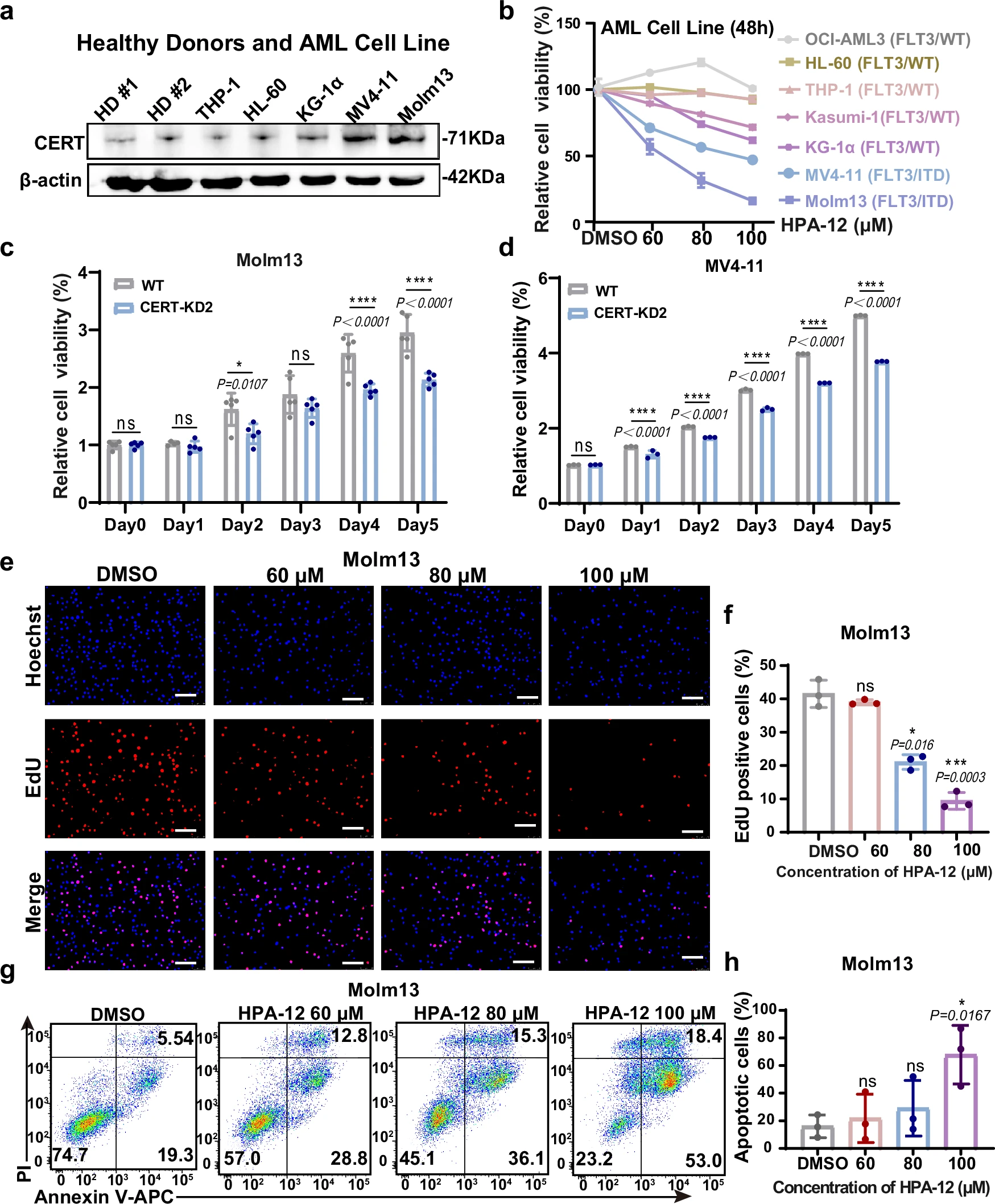
曾辉教授团队在《Nature Communications》上发表的研究揭示了靶向神经酰胺转运蛋白(CERT)可显著增强急性髓系白血病(AML)细胞对FLT3抑制剂的敏感性。研究发现,CERT在携带FLT3-ITD突变的AML细胞中高表达,靶向抑制CERT能够增加神经酰胺(Cer)积累,从而激活内质网应激-GRP78/ATF6/CHOP轴和线粒体自噬,协同抑制AML细胞增殖并诱导凋亡。此外,CERT抑制剂(如HPA-12)与FLT3抑制剂(如Crenolanib)联合使用,在体外和动物模型中展现出显著的协同效应,延长了生存时间,为克服FLT3抑制剂耐药提供了新策略。
推荐产品
参考文献
[1]IL-27 elicits a cytotoxic CD8 + T cell program to enforce tumour control.Nature,2025 Feb 05
[2]Endothelial insulin resistance induced by adrenomedullin mediates obesity-associated diabetes.Science,2025 Feb 07
[3]Homeobox C4 transcription factor promotes adipose tissue thermogenesis.Diabetes,2025 Jan 24
[4]GITRL enhances cytotoxicity and persistence of CAR-T cells in cancer therapy.Mol Ther,2025 Jan 25
[5]Lactate dehydrogenase B noncanonically promotes ferroptosis defense in KRAS-driven lung cancer.Cell Death Differ,2024 Dec 07
[6]MFGE8 induces anti-PD-1-therapy resistance by promoting extracellular vesicle sorting of PD-L1.Cell Rep Med,2025 Jan 16
[7]The lactate receptor HCAR1 drives the recruitment of immunosuppressive PMN-MDSCs in colorectal cancer.Nat Immunol,2025 Feb 04
[8]FBP1 controls liver cancer evolution from senescent MASH hepatocytes.Nature,2025 Jan
[9]Targeting CERT sensitizes AML Cells to FLT3 Inhibitors through activating GRP78-ATF6-CHOP Axis .Nat Commun,2025 Feb 04
*免责声明:华美生物内容团队仅是分享和解读公开研究论文及其发现,本文仅作信息交流,文中观点不代表华美生物立场,请理解。
应用:结直肠癌、肺癌等癌症潜在治疗靶点
来源:IL-27 elicits a cytotoxic CD8 + T cell program to enforce tumour control.Nature,2025 Feb 05

图源:10.1038/s41586-024-08510-w[1]
IL-27是一种关键的免疫调节因子,在肿瘤免疫治疗中展现出巨大潜力。研究表明,IL-27通过直接作用于肿瘤特异性CD8+ T细胞,增强其在肿瘤微环境中的持久性和效应功能,从而提升抗肿瘤免疫反应。在小鼠模型中,过表达IL-27或使用半衰期延长的IL-27蛋白可有效诱导肿瘤消退,且未观察到明显的免疫相关毒性。此外,IL-27与PD-L1抑制剂联合使用可显著增强治疗效果,为克服肿瘤免疫逃逸和耐受提供了新策略。临床数据进一步表明,IL-27的高表达与抗PD-1/PD-L1治疗的积极反应相关。这些发现揭示了IL-27在抗肿瘤免疫中的核心作用,并为其作为单一疗法或联合免疫治疗的临床应用奠定了重要基础。
02.靶点: CALCRL
应用:治疗2型糖尿病和肥胖相关代谢疾病的潜在靶点
来源:Endothelial insulin resistance induced by adrenomedullin mediates obesity-associated diabetes.Science,2025 Feb 07

图源:10.1126/science.adr4731[2]
《Science》杂志的一项新研究揭示了糖尿病的“隐形推手”——肾上腺髓质素(adrenomedullin)。该激素通过抑制血管内皮细胞的胰岛素信号传导,导致肥胖相关2型糖尿病患者的全身性胰岛素抵抗。研究发现,肾上腺髓质素激活Gαs-PKA-PTP1B信号通路,抑制胰岛素受体磷酸化,从而引发内皮胰岛素抵抗。在肥胖状态下,脂肪细胞大量分泌肾上腺髓质素,加剧了这一过程。通过阻断肾上腺髓质素受体,可以改善肥胖引起的胰岛素抵抗,为肥胖相关代谢疾病提供了新的治疗靶点。此外,内皮细胞可能成为多种疾病中胰岛素抵抗的共同节点,靶向内皮胰岛素信号通路具有广泛的治疗潜力。
03.靶点:HOXC4
应用:肥胖相关代谢疾病(如2型糖尿病)和胰腺癌的潜在治疗靶点
来源:Homeobox C4 transcription factor promotes adipose tissue thermogenesis.Diabetes,2025 Jan 24

来源:10.2337/db24-0675[3]
首都医科大学江梦溪课题组在《Diabetes》杂志发表研究,揭示了同源盒C4(HOXC4)在脂肪产热中的关键作用。全球肥胖症患者已超十亿,肥胖症与多种慢性代谢性疾病密切相关。HOXC4基因在棕色脂肪组织中高度富集,但其调节脂肪产热的机制尚不明确。研究通过生物信息学分析发现HOXC4相关基因富集于代谢通路,且与多项代谢指标相关。小鼠模型显示HOXC4表达量与体重负相关,与产热关键基因UCP1表达水平正相关。HOXC4通过与辅因子NCOA1相互作用,促进UCP1转录与脂肪产热,增强小鼠抗寒能力,并改善高脂饮食诱导的肥胖与胰岛素抵抗。该研究为肥胖相关代谢疾病治疗提供了新靶点与理论依据。04.靶点:GITRL
应用:可用于开发针对实体肿瘤的新型CAR-T细胞疗法
来源:GITRL enhances cytotoxicity and persistence of CAR-T cells in cancer therapy.Mol Ther,2025 Jan 25

图源:10.1016/j.ymthe.2025.01.036[4]
华东师范大学杜冰教授团队在《Molecular Therapy》发表研究,发现过表达GITRL的CAR-T细胞能显著增强实体肿瘤治疗效果。CAR-T疗法在血液恶性肿瘤治疗中取得突破,但在实体瘤治疗中效果不佳。GITR/GITRL信号能增强T细胞存活、增殖及杀伤功能。研究显示,过表达GITRL的CAR-T细胞可促进T细胞向抗肿瘤表型分化,增强激活及杀伤能力,促进增殖和Th9细胞分化,降低Treg细胞比例和耗竭。在前列腺癌动物模型中,过表达GITRL的CAR-T细胞延长了小鼠生存期,提升了持久性,且安全性较高。
05.靶点:LDHB
应用:治疗KRAS突变非小细胞肺癌(NSCLC)的潜在靶点
来源:Lactate dehydrogenase B noncanonically promotes ferroptosis defense in KRAS-driven lung cancer.Cell Death Differ,2024 Dec 07

LDHB沉默会损害KRAS依赖的非小细胞肺癌细胞中的谷胱甘肽代谢
图源:10.1038/s41418-024-01427-x[5]
图源:10.1038/s41418-024-01427-x[5]
瑞士伯尔尼大学附属小岛医院研究团队在《Cell Death & Differentiation》杂志发表的研究发现乳酸脱氢酶B(LDHB)在KRAS驱动的非小细胞肺癌中通过非经典途径促进对铁死亡的抵抗。研究通过多组学整合分析,证实LDHB不仅参与乳酸-丙酮酸循环,还能调控谷胱甘肽合成及线粒体氧化磷酸化,维持氧化还原稳态。抑制LDHB并联合阻断SLC7A11可加剧线粒体代谢紊乱,引发脂质过氧化升高,诱发铁死亡。体外实验与小鼠模型显示,该策略能显著抑制肿瘤增殖并延长生存期,为KRAS突变肺癌的代谢治疗提供新思路。
06.靶点:MFGE8
应用:治疗多种肿瘤相关耐药问题的潜在靶点
来源:MFGE8 induces anti-PD-1-therapy resistance by promoting extracellular vesicle sorting of PD-L1.Cell Rep Med,2025 Jan 16

图源:10.1016/j.xcrm.2024.101922[6]
浙江大学蔡志坚教授团队在《Cell Reports Medicine》杂志发表研究,揭示了MFGE8(乳脂球表皮生长因子8)在介导抗PD-1治疗耐药中的关键作用。研究发现,肿瘤细胞通过分泌MFGE8诱导PD-L1分选至胞外囊泡(TEVs),进而增强免疫抑制能力,导致抗PD-1治疗耐药。团队还发现,MFGE8通过激活αv整合素信号通路,上调UBE4A的表达,促进PD-L1的泛素化和分选至TEVs。在肿瘤进展过程中,MFGE8水平升高,进一步加剧了抗PD-1治疗的耐药性。
从临床转化角度来看,使用抗MFGE8中和抗体可以有效下调UBE4A和TEVs上的PD-L1,从而消除抗PD-1治疗耐药性。此外,肿瘤患者血清中MFGE8和PD-L1+ EV水平呈正相关,其高水平与抗PD-1治疗后的不良预后相关。因此,MFGE8不仅是一个有潜力的抗耐药靶点,还可作为预测抗PD-1治疗反应性的生物标志物。
07.靶点:HCAR1
应用:治疗结肠直肠癌及其他多种癌症的潜在靶点
来源:The lactate receptor HCAR1 drives the recruitment of immunosuppressive PMN-MDSCs in colorectal cancer.Nat Immunol,2025 Feb 04

图源:10.1038/s41590-024-02068-5[7]
华东师范大学生命科学学院卢伟强研究员和刘明耀教授团队在《Nature Immunology》杂志发表研究,揭示了G蛋白偶联受体家族成员HCAR1通过感知乳酸信号,驱动肿瘤免疫逃逸的新机制。研究发现,乳酸受体HCAR1信号通路的激活会诱导结肠直肠肿瘤细胞中趋化因子CCL2和CCL7的表达,从而招募免疫抑制性CCR2+多形核髓系来源的抑制细胞(PMN-MDSCs)进入肿瘤微环境。在结肠直肠癌小鼠模型中,敲除Hcar1基因显著降低了肿瘤浸润性CCR2+ PMN-MDSCs的数量,增强了CD8+ T细胞的活化,从而减轻了肿瘤负担。此外,FDA批准的药物利血平可抑制乳酸介导的HCAR1激活,削弱PMN-MDSCs的募集,增强CD8+ T细胞依赖的抗肿瘤免疫反应,并使免疫疗法耐药的肿瘤对PD-1抗体疗法敏感。该研究为理解乳酸介导的肿瘤免疫逃逸机制提供了新视角,并为开发肿瘤免疫创新疗法提供了新靶点和候选药物。
08.靶点:FBP1
应用:治疗肝细胞癌(HCC)的潜在靶点
来源:FBP1 controls liver cancer evolution from senescent MASH hepatocytes.Nature,2025 Jan

来源:10.1038/s41586-024-08317-9[8]
加州大学圣地亚哥分校的Michael Karin、Li Gu和Yahui Zhu团队在《Nature》杂志发表研究,揭示了FBP1(果糖-1,6-二磷酸酶1)在肝细胞癌(HCC)发生中的关键作用。研究发现,FBP1是一个p53靶基因,在代谢功能障碍相关脂肪性肝炎(MASH)诱导的衰老肝细胞中表达上调,但在大多数人类HCC中通过启动子高甲基化和蛋白酶体降解被抑制。
FBP1在代谢应激的癌前病变肝细胞和HCC祖细胞中率先下降,与AKT和NRF2的致癌激活同时发生。AKT和NRF2通过加速FBP1和p53的降解,增强了衰老HCC祖细胞的增殖和代谢活性。这种NRF2-FBP1-AKT-p53代谢开关不仅逆转了衰老,还促进了MASH向HCC的进展,并增强了DNA损伤诱导的体细胞突变积累。
该研究指出,FBP1的缺失是MASH向HCC进展的关键机制,为HCC的预防和治疗提供了新的靶点。
09.靶点:CERT
应用:治疗急性髓系白血病(AML)的潜在靶点
来源:Targeting CERT sensitizes AML Cells to FLT3 Inhibitors through activating GRP78-ATF6-CHOP Axis .Nat Commun,2025 Feb 04

HPA-12抑制CERT可降低AML细胞系的活性并促进其凋亡
图源:10.1038/s41467-025-56520-7[9]
曾辉教授团队在《Nature Communications》上发表的研究揭示了靶向神经酰胺转运蛋白(CERT)可显著增强急性髓系白血病(AML)细胞对FLT3抑制剂的敏感性。研究发现,CERT在携带FLT3-ITD突变的AML细胞中高表达,靶向抑制CERT能够增加神经酰胺(Cer)积累,从而激活内质网应激-GRP78/ATF6/CHOP轴和线粒体自噬,协同抑制AML细胞增殖并诱导凋亡。此外,CERT抑制剂(如HPA-12)与FLT3抑制剂(如Crenolanib)联合使用,在体外和动物模型中展现出显著的协同效应,延长了生存时间,为克服FLT3抑制剂耐药提供了新策略。
推荐产品
| 靶点 | 重组蛋白 | 货号 |
| IL27 | Recombinant Human Interleukin-27 subunit alpha (IL27) | CSB-MP847702HU |
| CALCRL | Recombinant Human Calcitonin gene-related peptide type 1 receptor (CALCRL), partial | CSB-MP614981HU1 |
| HOXC4 | Recombinant Human Homeobox protein Hox-C4 (HOXC4) | CSB-MP010675HU |
| GITRL | Recombinant Human Tumor necrosis factor ligand superfamily member 18 (TNFSF18), partial (Active) | CSB-MP891791HU |
| LDHB | Recombinant Human L-lactate dehydrogenase B chain (LDHB) | CSB-EP012841HUc7 |
| MFGE8 | Recombinant Human Lactadherin (MFGE8) | CSB-EP013752HU |
| HCAR1 | Recombinant Human Hydroxycarboxylic acid receptor 1 (HCAR1), partial | CSB-MP861159HU1 |
| FBP1 | Recombinant Human Fructose-1,6-bisphosphatase 1 (FBP1) | CSB-EP008459HU |
| CERT | Recombinant Human Collagen type IV alpha-3-binding protein (COL4A3BP) | CSB-MP896912HU |
参考文献
[1]IL-27 elicits a cytotoxic CD8 + T cell program to enforce tumour control.Nature,2025 Feb 05
[2]Endothelial insulin resistance induced by adrenomedullin mediates obesity-associated diabetes.Science,2025 Feb 07
[3]Homeobox C4 transcription factor promotes adipose tissue thermogenesis.Diabetes,2025 Jan 24
[4]GITRL enhances cytotoxicity and persistence of CAR-T cells in cancer therapy.Mol Ther,2025 Jan 25
[5]Lactate dehydrogenase B noncanonically promotes ferroptosis defense in KRAS-driven lung cancer.Cell Death Differ,2024 Dec 07
[6]MFGE8 induces anti-PD-1-therapy resistance by promoting extracellular vesicle sorting of PD-L1.Cell Rep Med,2025 Jan 16
[7]The lactate receptor HCAR1 drives the recruitment of immunosuppressive PMN-MDSCs in colorectal cancer.Nat Immunol,2025 Feb 04
[8]FBP1 controls liver cancer evolution from senescent MASH hepatocytes.Nature,2025 Jan
[9]Targeting CERT sensitizes AML Cells to FLT3 Inhibitors through activating GRP78-ATF6-CHOP Axis .Nat Commun,2025 Feb 04
*免责声明:华美生物内容团队仅是分享和解读公开研究论文及其发现,本文仅作信息交流,文中观点不代表华美生物立场,请理解。










