TNFSF15/TL1A:药企巨头抢滩布局,下一个百亿级靶点的崛起之路
日期:2025-02-07 08:53:16
近日,关于TNFSF15/TL1A的喜报频传。三生国健抗TL1A单抗SSGJ-627注射液IND申请获CDE受理,率先开启中国药企TL1A靶点临床研究;在第43届摩根大通年度医疗健康大会上,默沙东预估TL1A靶点自免治疗潜力达数十亿美元;梯瓦制药也对其抗TL1A单抗duvakitug临床数据表示满意。
在交易市场,TL1A靶点也是焦点。2023年,默沙东以108亿美元收购prometheus公司,其核心产品为靶向tl1a单抗; 赛诺菲与teva公司达成10亿美元合作,开发teva的tl1a抗体疗法tev'574; 12月,罗氏以71亿美元预付款收购telavant公司,获得rvt-3101在美国和日本的权益。2024年6月,明济生物与艾伯维达成约17.1亿美元合作,开发下一代tl1a抗体fg-m701用于治疗炎症性肠病。
TL1A靶点吸引众多药企竞相布局,其背后的原因值得深入探究。作为肿瘤坏死因子超家族重要成员,TL1A在免疫调节、炎症反应和肿瘤发生发展等关键生理病理过程中扮演核心角色。下面,就让我们从TL1A生物学特性、信号通路以及与相关疾病的关联等方面,深入探索TL1A在药物开发中的应用与进展。
1. 关于TNFSF15/TL1A
1.1 基因与蛋白结构
TNFSF15,即肿瘤坏死因子超家族成员15,又名TL1A,为Ⅱ型跨膜蛋白,由胞内区、跨膜区和胞外区构成。其中,胞外区含有保守的TNF同源结构域,这一结构域是TNFSF15与受体结合的关键部位,直接决定其生物学活性 [1]。此外,胞外区还可被酶解成可溶性形式,在生物体内发挥与膜结合形式不同的功能。
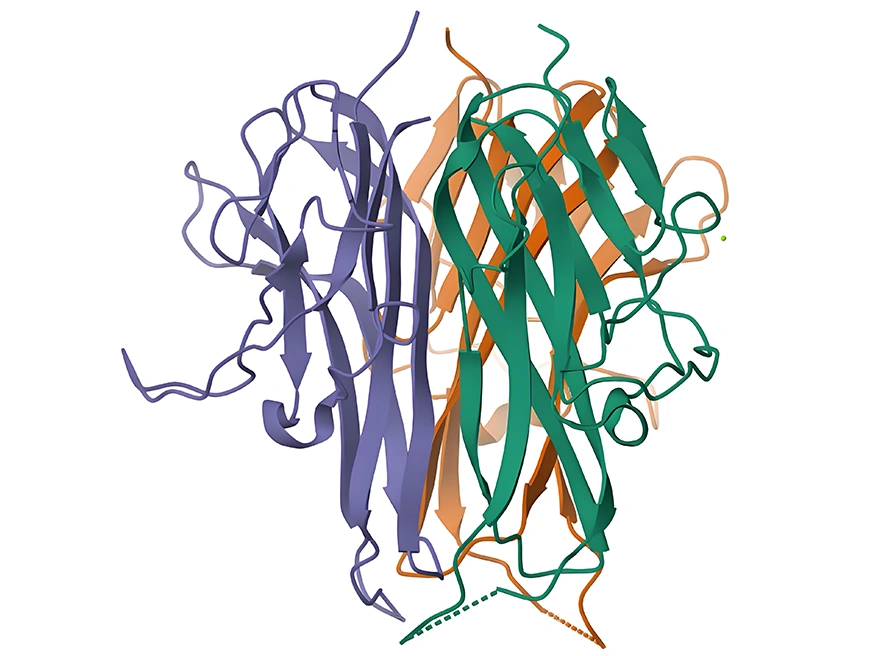
图 1:TNFSF15 蛋白结构示意图
(图源:PDB数据库)
TNFSF15 基因由5个外显子和4个内含子组成。其编码的蛋白在结构上,胞内区可能参与细胞内信号的起始和调控,跨膜区负责将蛋白锚定在细胞膜上,而胞外区的TNF同源结构域在与受体结合并激活下游信号传导中起决定性作用 [1,2]。不同物种间TNFSF15基因和蛋白序列具有一定保守性,暗示其功能重要性和进化上的保守性。
1.2 表达与调控机制
TNFSF15在多种免疫细胞,如T细胞、B细胞、单核细胞等中均有表达。其表达受多种因素精细调控,包括炎症因子、转录因子等。在炎症状态下,TNF-α、IL-1β等炎症因子可通过与细胞表面相应受体结合,激活细胞内信号通路,诱导TNFSF15表达上调,进而参与炎症反应的级联放大 [2,3]。此外,一些转录因子如NF-κB等,也可直接结合到TNFSF15基因启动子区域,调控其转录水平。
1.3 相关信号通路
TNFSF15主要通过与受体DR3结合来激活信号通路。二者结合后,招募衔接蛋白TRADD,进而激活NF-κB和MAPK 等多条信号通路。NF-κB信号通路的激活可促进一系列炎症因子、抗凋亡蛋白等的表达,影响细胞的存活、增殖和炎症反应;而MAPK信号通路则在细胞增殖、分化和凋亡等过程中发挥重要调控作用 [2,3]。
2. TNFSF15/TL1A 与疾病的关联
2.1 TNFSF15/TL1A与自身免疫性疾病
● 炎症性肠病
炎症性肠病(IBD)主要包括克罗恩病和溃疡性结肠炎,是一类病因尚不明确的慢性非特异性肠道炎症性疾病。大量研究表明,TNFSF15基因多态性与IBD易感性密切相关 [7]。在IBD患者的肠道组织中,TNFSF15表达显著升高。从作用机制看,TNFSF15通过其DR3受体在肠道炎症级联和纤维化中起关键作用 。它通过激活NF-κB信号通路,促使炎症因子如IL6、IL8、TNF-α等大量释放,引发肠道黏膜的炎症损伤和免疫紊乱 [3,7]。临床研究发现,IBD患者血清和肠道黏膜中TNFSF15水平与疾病活动度呈正相关,可作为评估疾病严重程度和预后的潜在生物标志物。
多项遗传学研究对不同种族IBD患者进行分析,均发现TNFSF15基因特定单核苷酸多态性(SNP)位点与疾病风险增加相关 [7]。在动物实验中,敲除TNFSF15基因或阻断其信号通路,可显著减轻实验性结肠炎小鼠的肠道炎症症状,表现为肠道黏膜损伤减轻、炎症因子表达降低等。并且,使用中和TNFSF15抗体可有效逆转结肠纤维化,使其恢复到最初的炎症前水平,这种逆转可能归因于结缔组织生长因子、IL31Ra、TGF-β1和IGF-1的表达减少 。
● 类风湿关节炎
类风湿关节炎是一种以关节滑膜炎症为主要特征的自身免疫性疾病,可导致关节疼痛、肿胀、畸形,严重影响患者生活质量。在类风湿关节炎患者体内,TNFSF15 水平明显升高 [4]。其可刺激滑膜细胞增殖,促进炎症因子如 IL-1、IL-6、TNF-α等的分泌,这些炎症因子进一步激活免疫细胞,形成炎症恶性循环,导致关节软骨和骨质破坏 [4]。研究还发现,TNFSF15可通过诱导破骨细胞分化和活化,加速关节骨质吸收,加重关节损伤。临床研究表明,类风湿关节炎患者血清TNFSF15水平与疾病活动指数、关节破坏程度相关 [4]。
2.2 TNFSF15/TL1A与肿瘤
● 对肿瘤血管生成的影响
肿瘤的生长和转移依赖于充足的血液供应,血管生成在这一过程中起着关键作用。TNFSF15可通过调节血管内皮生长因子(VEGF)等血管生成因子的表达,促进肿瘤血管生成 [5,8]。研究发现,TNFSF15可激活肿瘤细胞或肿瘤微环境中的相关信号通路,上调VEGF的表达和分泌 [5,8]。VEGF与其受体结合后,可促进血管内皮细胞的增殖、迁移和管腔形成,为肿瘤生长和转移提供营养支持。在多种实体肿瘤如乳腺癌、肺癌、结直肠癌中,均观察到TNFSF15与肿瘤血管生成的密切关联。
临床研究表明,肿瘤组织中TNFSF15表达水平与肿瘤微血管密度呈正相关,高表达TNFSF15的肿瘤患者往往预后较差 [8]。在动物实验中,抑制TNFSF15的功能可显著减少肿瘤血管生成,抑制肿瘤生长和转移。
● 与肿瘤免疫微环境
肿瘤免疫微环境是肿瘤细胞与免疫细胞、间质细胞及细胞外基质等共同构成的复杂生态系统。TNFSF15在肿瘤免疫微环境中发挥着双重调节作用 [6]。一方面,TNFSF15可激活T细胞和NK细胞,增强机体的抗肿瘤免疫反应 [6]。它可促进T细胞的增殖、分化和细胞因子分泌,增强T细胞对肿瘤细胞的杀伤活性;同时,也可激活NK细胞,使其发挥更强的细胞毒性作用。另一方面,在某些肿瘤微环境中,TNFSF15可诱导免疫抑制细胞如调节性T细胞(Treg)和髓源性抑制细胞(MDSC)的产生和聚集,促进肿瘤免疫逃逸。
临床研究发现,在部分肿瘤患者中,肿瘤组织中TNFSF15的表达水平与Treg细胞浸润呈正相关,与肿瘤患者的不良预后相关 [6]。而在另一些肿瘤中,高表达的TNFSF15则与较好的免疫浸润和预后相关 [6]。这提示TNFSF15在肿瘤免疫微环境中的作用可能因肿瘤类型、分期和个体差异而有所不同。
3. TNFSF15/TL1A 相关药物研发进展
目前,已有多款靶向TNFSF15的抗体药物进入临床试验阶段。这些抗体药物主要通过特异性地结合TNFSF15,阻断其与受体DR3的相互作用,从而抑制下游信号传导,达到治疗疾病的目的。主要适应症为溃疡性结肠炎、克罗恩病等,最高研究阶段临床3期。部分整理如下表:
| 药物 | 药物类型 | 在研适应症 | 在研机构 | 最高研发阶段 |
|---|---|---|---|---|
| Afimkibart | 单克隆抗体 | 活动性中度溃疡性结肠炎 | 活动性重度溃疡性结肠炎 | 溃疡性结肠炎 | 克罗恩病 | Hoffmann-La Roche, Inc. | F. Hoffmann-La Roche Ltd. | Hoffmann-La Roche Ltd. | Roivant Sciences Ltd. | Roche Holding AG | 临床3期 |
| Tulisokibart | 单克隆抗体 | 克罗恩病 | 溃疡性结肠炎 | 弥漫性硬皮病 | 系统性硬化相关的间质性肺病 | 活动性中度溃疡性结肠炎 | 活动性重度溃疡性结肠炎 | Prometheus Biosciences, Inc. | Merck Sharp & Dohme Corp. | Merck Sharp & Dohme LLC | 默沙东研发(中国)有限公司 | 临床3期 |
| Duvakitug | 单克隆抗体 | 溃疡性结肠炎 | 克罗恩病 | Sanofi | Teva Branded Pharmaceutical Products R&D, Inc. | 临床2期 |
| XmAb942(Xencor) | 单克隆抗体 | 溃疡性结肠炎 | Xencor, Inc. | 临床1/2期 |
| BCD-261 | 单克隆抗体 | - | Biocad CJSC | 临床1期 |
| PF-07261271 | 双特异性抗体 | 炎症性肠病 | Pfizer Inc. | 临床1期 |
| SPY-002 | 单克隆抗体 | 炎症性肠病 | Spyre Therapeutics, Inc. | 临床1期 |
| SSGJ-627 | 单克隆抗体 | - | 三生国健药业(上海)股份有限公司 | 临床申请 |
在自身免疫性疾病方面,初步临床试验结果显示,这些靶向TNFSF15的抗体药物具有较好的疗效和安全性。例如,在炎症性肠病的临床试验中,使用这些抗体药物治疗后,患者的肠道炎症症状得到明显改善,疾病活动度降低,且不良反应轻微。
在肿瘤治疗领域,虽然靶向TNFSF15的抗体药物仍处于探索阶段,但已有研究表明,其与其他抗肿瘤治疗方法如化疗、免疫治疗联合使用,可增强抗肿瘤效果 [1,2]。
4. TNFSF15/TL1A研究相关产品推荐
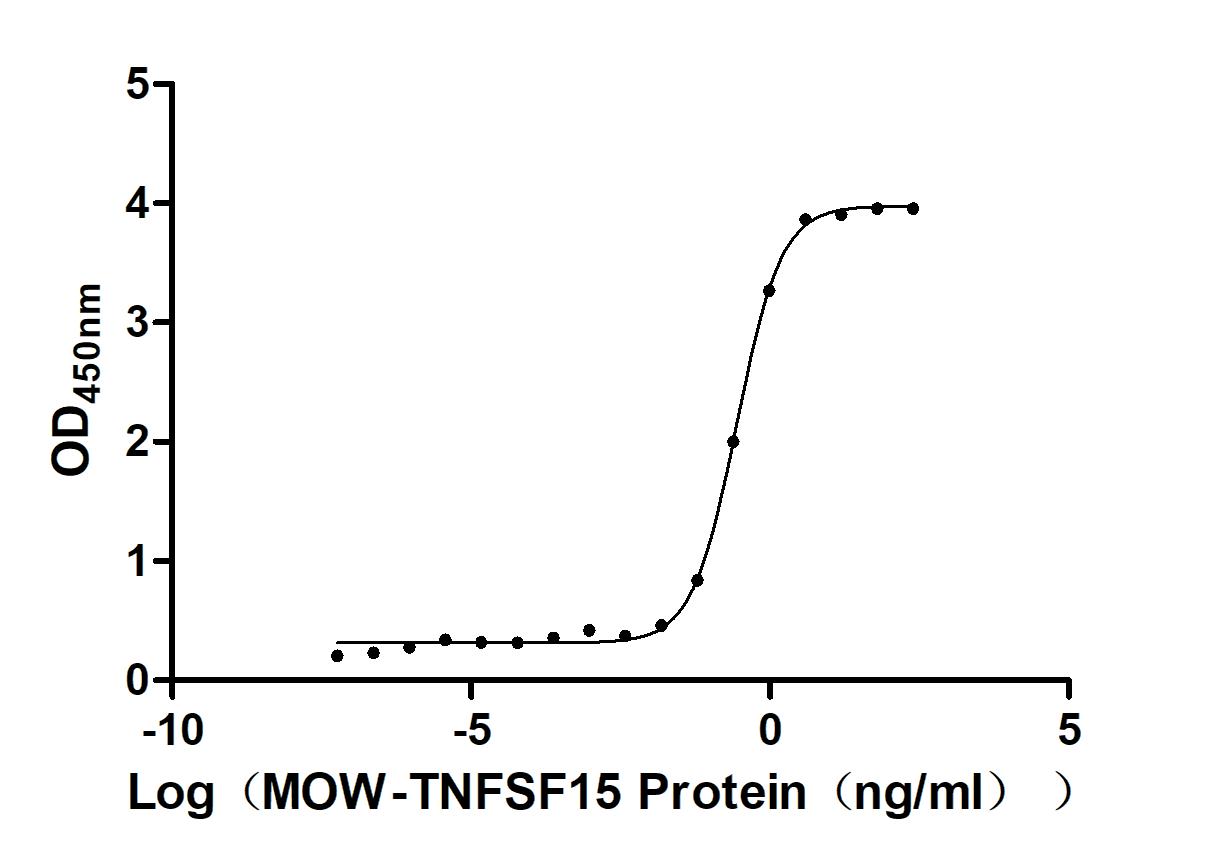
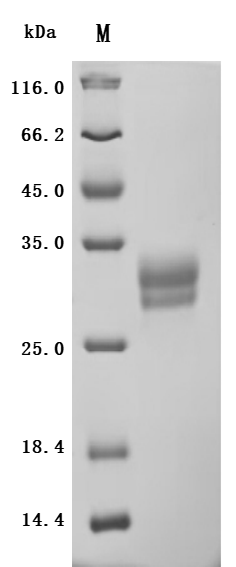
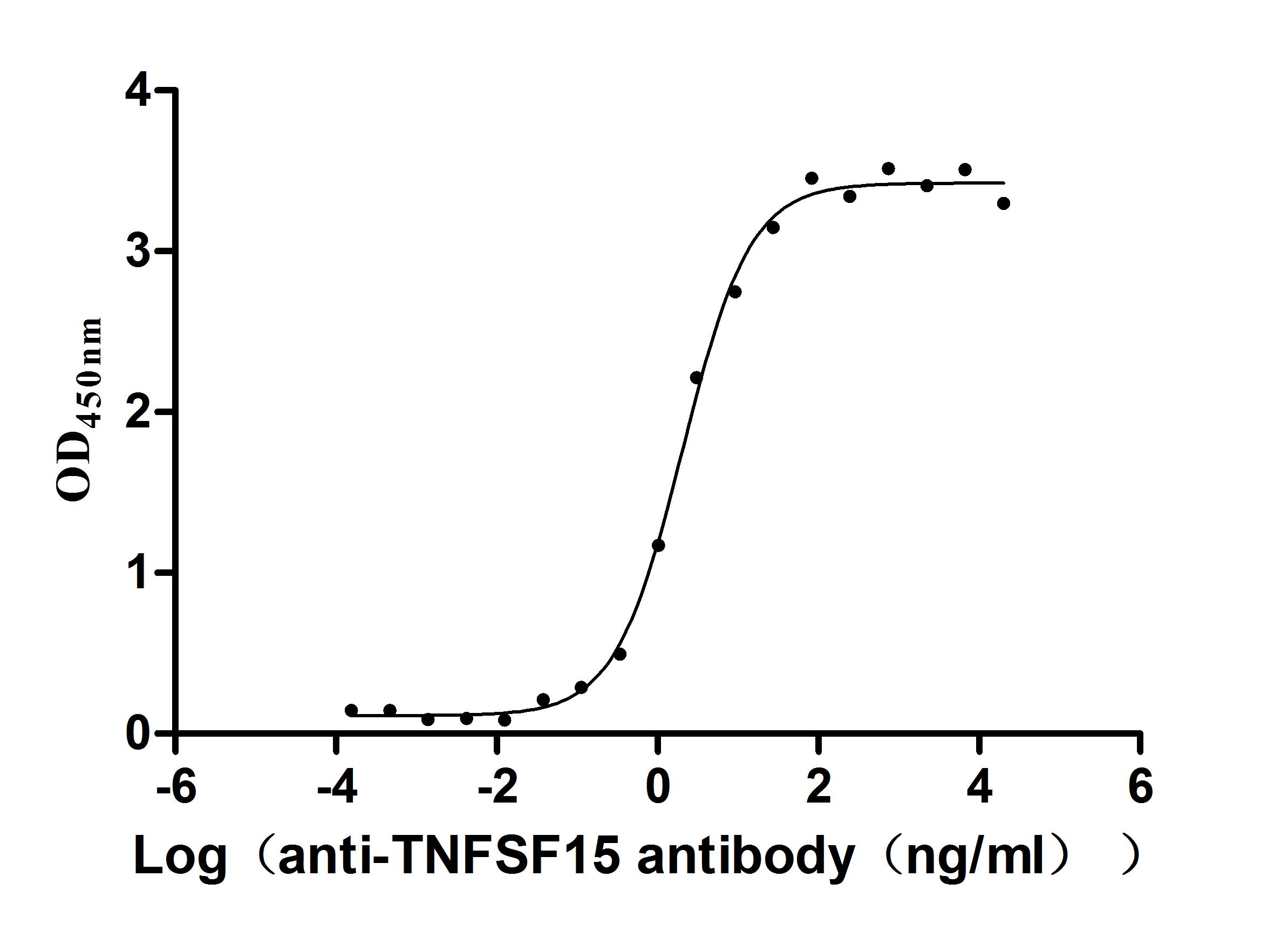
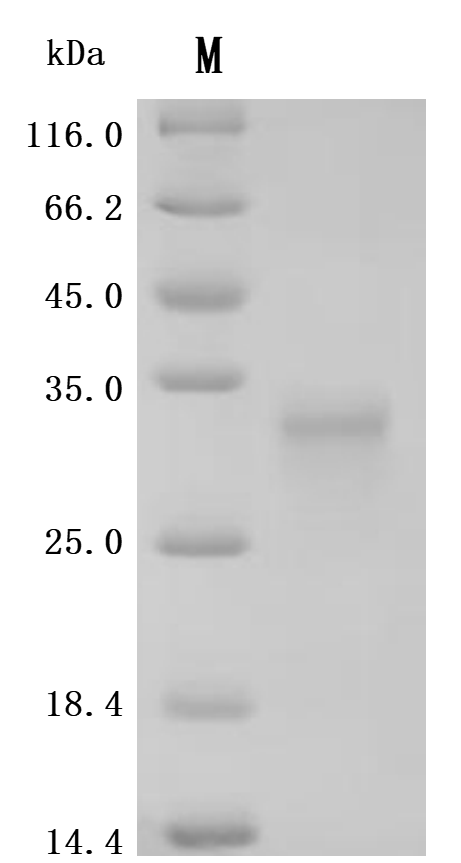
为助力各药企及科研机构研发人员对TNFSF15/TL1A 的研究,华美生物重磅推出多款高活性的TNFSF15/TL1A蛋白产品,覆盖人、小鼠、猴等多种属,并提供TNFSF15/TL1A 抗体及ELISA试剂盒产品,助力您在TNFSF15/TL1A机制方面的研究或其潜在临床价值的探索。
● TNFSF15/TL1A 重组蛋白
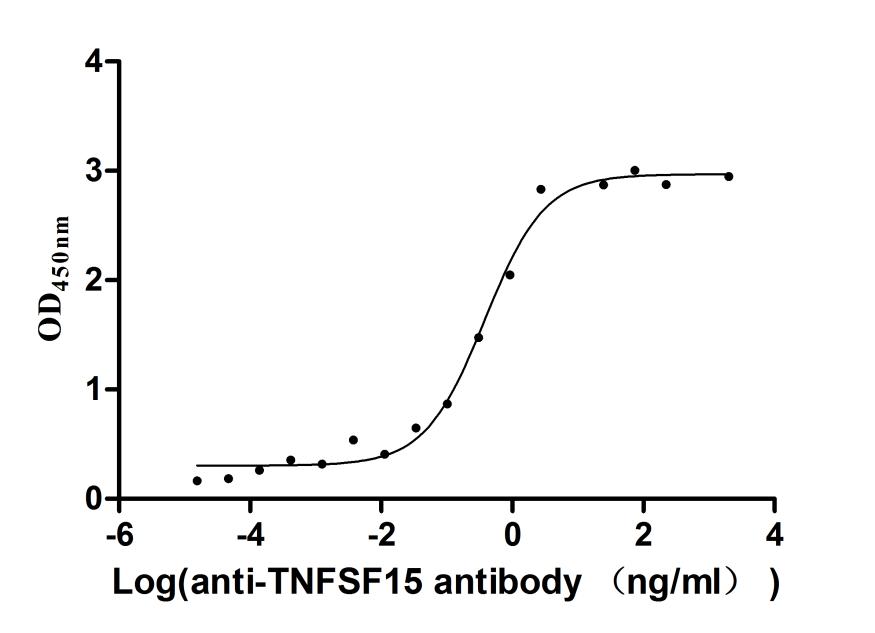
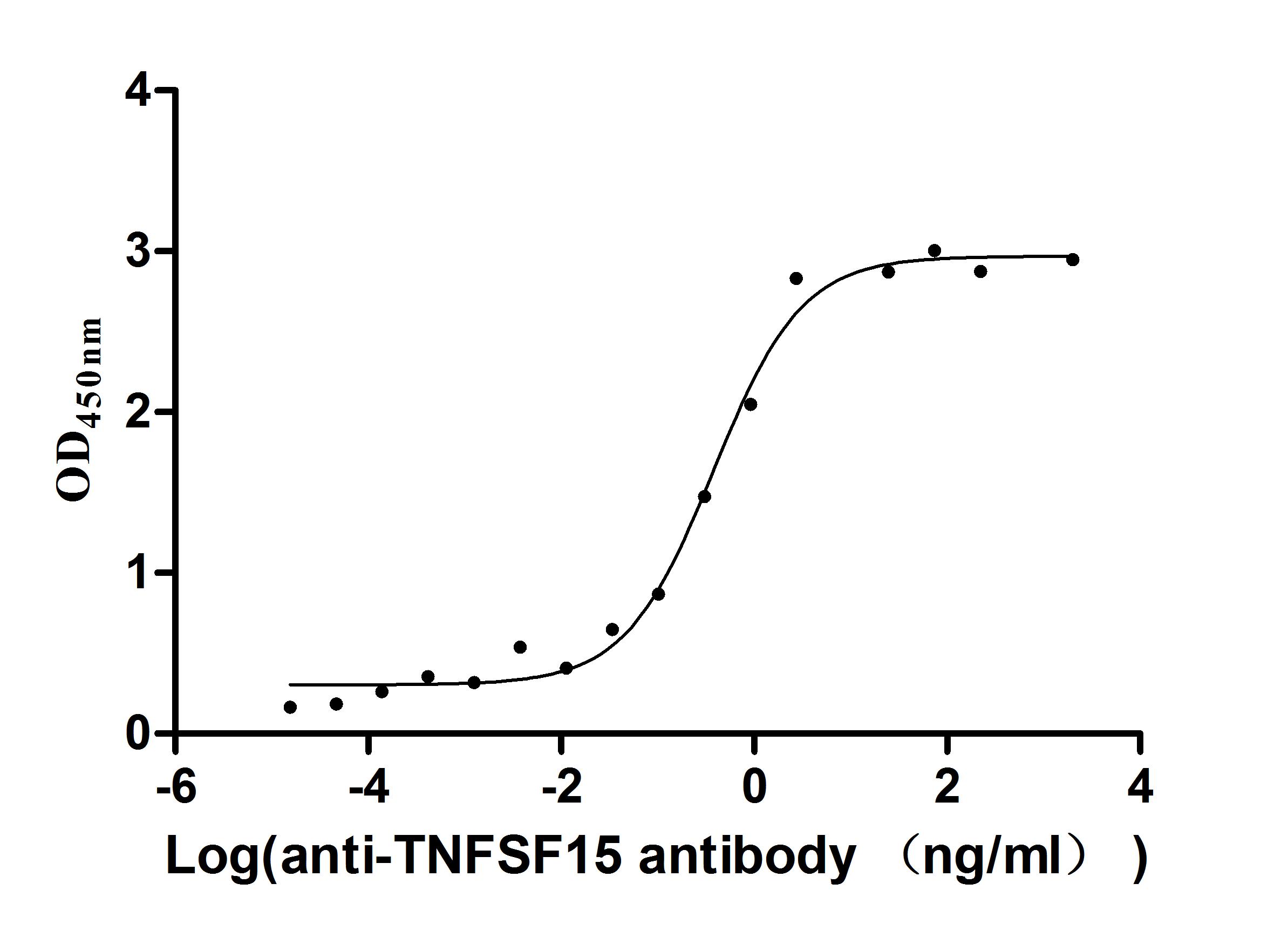
● TNFSF15/TL1A 抗体
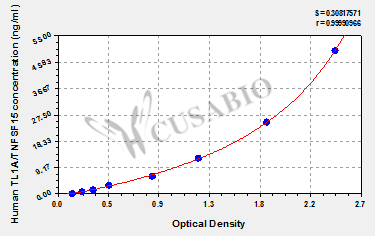
● TNFSF15/TL1A 酶免试剂盒
点击查看TNFSF15/TL1A所有相关产品
参考文献:
[1] Smith CA, Farrah T, Goodwin RG. The TNF receptor superfamily of cellular and viral proteins: activation, costimulation, and death. Cell. 1994;76(6):959 - 962.
[2] Aggarwal BB. Signaling pathways of the TNF - superfamily: a double - edged sword. Nat Rev Immunol. 2003;3(9):745 - 756.
[3] Neurath MF. TNFalpha in inflammatory bowel disease: friend or foe? Trends Mol Med. 2003;9(11):518 - 524.
[4] Chabaud M, Fossiez F, Taupin JL, et al. Overexpression of interleukin - 15 in rheumatoid synovium and in interleukin - 1 - stimulated rheumatoid synovial fibroblasts. Arthritis Rheum. 1996;39(4):681 - 689.
[5] Ferrara N, Gerber HP, LeCouter J. The biology of VEGF and its receptors. Nat Med. 2003;9(6):669 - 676.
[6] Dunn GP, Bruce AT, Ikeda H, Old LJ, Schreiber RD. Cancer immunoediting: from immunosurveillance to tumor escape. Nat Immunol. 2002;3(11):991 - 998.
[7] Zhang X, Li Y, Wang Y, et al. TNFSF15 polymorphisms and susceptibility to inflammatory bowel disease: a meta - analysis. Inflamm Bowel Dis. 2012;18(10):1864 - 1873.
[8] Yang Z, Wang Y, Li Y, et al. TNFSF15 promotes angiogenesis in colorectal cancer by upregulating VEGF expression. Oncol Rep. 2015;33(2):671 - 673.


-AC1.jpg)
-SDS.jpg)